近日,山东大学刘新泳教授团队依托山东省中比抗病毒创新药物合作研究中心、化学生物学教育部重点实验室等科研平台,针对抗病毒药物研究领域的关键科学问题,在科技部、国家自然科学基金国际合作重点项目及面上项目以及山东省重大创新工程等项目的持续资助下,一方面针对新靶标,发现新结构和新机制抗病毒先导化合物,为药物开发提供战略储备;另一方面通过对上市药物的结构优化,发现新一代高效抗耐药性候选药物。3篇研究成果连续在药物化学顶尖期刊《药物化学杂志》(Journal of Medicinal Chemistry)发表。另外,刘新泳教授团队还针对16种致病性病毒的药物研究现状撰写了19篇文章,在《药学学报》以专刊形式发表。
基于靶标结构发现新型HIV-1衣壳蛋白抑制剂。发现新靶标新机制抑制剂可从根本上克服现有临床抗病毒药物的耐药性问题。衣壳蛋白(Capsid protein,CA)在HIV-1复制周期的早期和晚期中多个环节均发挥着重要作用,同时成熟的CA还可以保护内部的病毒基因免受外界破坏,因此CA成为抗HIV-1药物研究的新靶点。
近日,刘新泳教授团队以HIV-1衣壳蛋白六聚体相邻亚基蛋白界面为靶标,构建基于苯丙氨酸优势片段的化合物库,经体外细胞水平的抗病毒活性筛选(HIV-1NL4-3/TZM-bl细胞;HIV-1IIIB、HIV-2ROD/MT-4细胞)及机制研究发现了一系列新颖的苯丙氨酸类衣壳蛋白抑制剂。其中,化合物11l抗HIV-1活性最佳(EC50NL4-3= 90 nM;EC50IIIB= 0.21 μM)。此外,化合物11l具有显著的抗HIV-2ROD活性(EC50= 31 nM),安全性也大幅提高(SI:5768)。SPR实验表明,11l与CA六聚体具有较高的亲和力。进一步的机制实验表明,在病毒复制晚期,11l通过干扰HIV-1 CA组装产生传染性较小的病毒颗粒来发挥作用(IC50=8.96 nM);而在复制早期,11l通过选择性结合到HIV-1 CA起作用(IC50=0.24μM),加速病毒脱壳,使其与逆转录过程不相容。此外,11l具有良好的人血浆和肝微粒体稳定性、大鼠药代性质(口服生物利用度F=23%)和安全性。以上结果显示了以HIV-1 CA为靶点的抗艾滋病药物研发的前景。
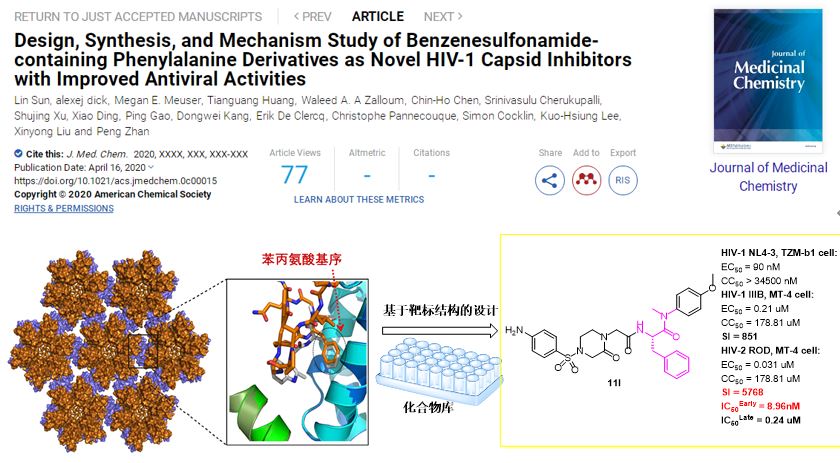
上述研究成果已在线发表于药物化学领域国际顶尖期刊Journal of Medicinal Chemistry(J Med Chem. 2020 Apr 16. doi: 10.1021/acs.jmedchem.0c00015.),第一作者为山东大学药学院在读博士生孙林,刘新泳教授、展鹏副教授、北卡罗来纳大学Kuo-Hsiung Lee教授及德雷克塞尔大学Simon Cocklin教授为本论文的共同通讯作者。目前,该成果已申请多项中国发明专利。
以HIV逆转录酶为靶标的抗艾滋病候选药物的发现。非核苷类HIV-1逆转录酶抑制剂(NNRTIs)具有高效、低毒等优点,是cART疗法的重要组成部分。然而该类药物极易产生耐药性,因此研发新一代非核苷类抗艾滋病药物的研发刻不容缓。HIV-1逆转录酶柔性强、存在诱导契合效应,给抗耐药性药物的合理设计带来很大挑战。
为此,刘新泳教授团队根据逆转录酶结构生物学特征指导结构优化,得到化合物24b和9a,对HIV-1野生株和临床常见突变株均具有纳摩尔水平的抑制活性(EC50分别为:3.60 - 21.5 nM;2.05-7.59 nM),优于上市药物依曲韦林。此外,化合物24b的细胞毒性很低(CC50> 155 μM),对HIV-1野生株和突变株均具有很高的选择性指数。在hERG钾通道抑制试验中,24b对hERG抑制活性大幅降低(IC50> 30 μM),远远优于同类上市药物利匹韦林(IC50< 1 μM),心脏安全性大幅提升。表型交叉耐药性实验发现,9a不会导致不同机制抑制剂的交叉抗耐药性;9a具有良好的大鼠口服生物利用度(F= 37.06%)与安全性(LD50> 2000 mg/kg)。24b和9a是值得开发的优质候选药物,有望作为cART疗法的组分与NRTIs联手用于艾滋病的治疗。
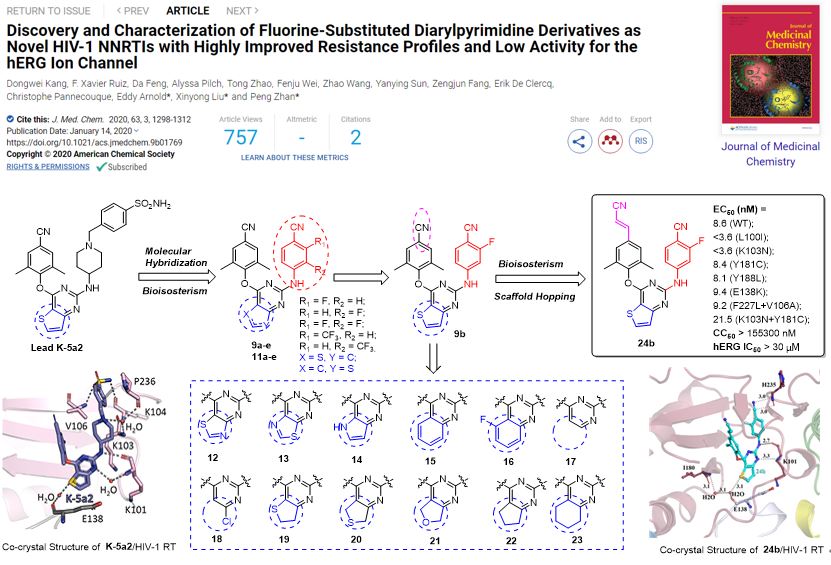
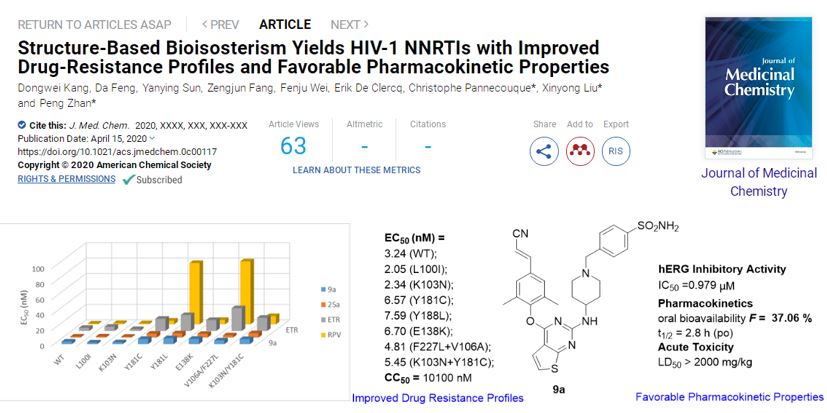
上述研究成果已连续在Journal of Medicinal Chemistry发表2篇文章(J Med Chem.2020,63, 1298-1312;J Med Chem.2020 Apr 15. doi: 10.1021/acs.jmedchem.0c00117.),第一作者均为山东大学特别资助类博士后康东伟;山东大学药学院刘新泳教授、展鹏副教授均为两篇文章的共通讯作者;罗格斯大学Eddy Arnold教授及比利时鲁汶大学Christophe Pannecouque教授分别为两篇论文的共同通讯作者。
在《药学学报》发表抗病毒药物化学研究进展专刊。在抗病毒药物先导化合物及候选药物的研究过程中,刘新泳教授团队发展了一系列抗病毒药物研究共性方法与技术。疫情当下,本团队在应急药物研发的同时,根据国内外抗病毒药物研究领域的新动向,针对各种不同病毒药物研究新进展,从药物化学的视角,分析抗病毒药物研究的成功经验,探求药物研发的内在规律,共撰写19篇文章,涵盖冠状病毒、乙肝病毒、丙肝病毒、流感病毒、埃博拉病毒、呼吸道合胞病毒、肠病毒、西尼罗病毒、登革病毒、腺病毒、寨卡病毒、人巨细胞病毒、疱疹病毒、痘病毒、基孔肯雅病毒、诺如病毒。以《抗病毒药物化学研究进展专刊》为题发表在2020年第4期的《药学学报》(http://www.yxxb.com.cn:8081/aps/CN/volumn/current.shtml#综述)。专刊发表后,部分被推荐为优秀论文,将由中国知网进行全文翻译,以中英双语对照网络版的方式在海外宣传推广。
相关链接:
https://pubs.acs.org/doi/10.1021/acs.jmedchem.0c00015
https://pubs.acs.org/doi/10.1021/acs.jmedchem.9b01769
https://pubs.acs.org/doi/10.1021/acs.jmedchem.0c00117
